Tartalom
Az atomspektroszkópia az optikai spektroszkópiai módszerek csoportjába tartozó olyan analitikai eljárás, mellyel az anyagok elemi összetételét határozhatjuk meg. Az atomspektroszkópiához három módszer tartozik: az emissziós, az abszorpciós és a fluoreszcens módszer. Mindhárom esetben az anyagot nagy hőmérsékletű gázállapotban vizsgáljuk. A módszerek egyik előnye, hogy viszonylag egyszerű berendezésekkel ppm, sőt egyes esetekben ppb koncentrációtartományban vizsgálódhatunk.
Az emisszió során a gerjesztett állapotba került atom fölös energiáját fény formájában kibocsátja, miközben visszatér alapállapotba.
Ez a jelenség figyelhető meg akkor is, amikor az alkálifémek, illetve az alkáliföldfémek vegyületei megfestik a gázlángot, ugyanis ezek az elemek már viszonylag alacsony hőmérsékleten is könnyen gerjeszthetők (A lítium bíborvörösre, a nátrium sárgára, a kálium fakóibolyára, a kalcium téglavörösre, a bárium sárgászöldre festi a Bunsen-égő lángját). A megfigyeléseinket kézi spektroszkóp használatával pontosíthatjuk. A spektroszkópba belépő fény egy lencsén keresztül annak prizmáján (monokromátorán) különböző hullámhosszúságú összetevőire bomlik. Ekkor a spektroszkóp nézőkéjében az emittált fény színképét (spektrumát) láthatjuk, miközben a spektrumban megjelenő színes vonalak hullámhosszát is leolvashatjuk. A kibocsátott fény hullámhosszából a fény energiája kiszámítható:
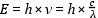
ahol λ = a fény hullámhossza h = arányossági tényező a
Planck-féle állandó (6.63×10-34 Js) ν = a
fény frekvenciája c = a fény sebessége vákuumban (≈
3×108 m/s)
Az emissziós vizsgálatokhoz szükséges gerjesztett állapotú atomokat többféle módon (lángban, ívben, szikrában) előállíthatjuk. A FES-nél a lángban történik a minta atomizálása (a minta atomos gőzzé alakítása), valamint az így képződött szabad atomok termikus gerjesztése is.
A mérés első lépésében a vizsgálandó mintából oldatot készítünk, majd ezt beporlasztjuk a lángba. A porlasztás során keletkező apró cseppek mérete függ az oldószertől és a porlasztó felépítésétől. A lángba bejutott cseppek több lépésben a hőenergia hatására átalakulnak, szabad atomok keletkeznek, melyek megfelelő energia hatására gerjesztődhetnek is. Az atomok gerjesztett állapota foton emisszió útján szűnik meg. A kibocsátott fény hullámhossza (energiája) az atom elektronszerkezetétől függ, míg az adott hullámhosszon a fény intenzitása a gerjesztett atomok koncentrációjával, közvetve pedig az oldat elemkoncentrációjával arányos.
Az atomabszorpciós spektrométerek felépítése, melyek használhatók lángemissziós spektrométerként is, az 5.1. ábrán látható. A vizsgált minta a mintabeviteli egység segítségével a lángba (atomizáló egységbe) kerül. A monokromátor a fény felbontását szolgálja, míg a fény detektálása fotoelektron-sokszorozóval történik. A detektált adatok feldolgozását, rögzítését a jelfeldolgozó elektronika és a kijelző rendszer végzi. Az 5.1. ábrán látható fényforrást a lángatomabszorpciós spektrometriánál (FAAS) alkalmazzuk, a FES méréseknél nincs rá szükség.
A lángemissziós spekrometria a láng viszonylag alacsony hőmérséklete miatt elsősorban a kis gerjesztési energiájú alkáli- és alkáliföldfémek elemzésére alkalmas. Gyors, egyszerű, és könnyen automatizálható technika. Különösen a környezetvédelemben (pl. vízanalitika), a biológiai analízisekben és az orvosi diagnosztikában terjedt el. Magasabb hőmérsékletű lángok használatával (C2H2/N2O láng; ~3000°C) a módszer alkalmazási területe kiterjeszthető.
Az atomspektroszkópiás módszerek pontosságát, érzékenységét nagyban befolyásolja, hogy milyen a mintabevitel sebessége, hatásfoka, illetve reprodukálhatósága. A minták halmazállapotától és az atomizáló tér milyenségétől (láng vagy grafitkemence) függően különböző mintabeviteli technikák alakultak ki.
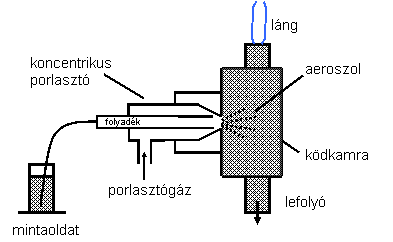
A folyékony halmazállapotú mintát leggyakrabban porlasztás segítségével juttatjuk be a lángba. Erre a pneumatikus porlasztás a legelterjedtebb és egyben a legrégebbi módszer. A porlasztás során a folyadékból nagy sebességű gázáram segítségével mikroméretű (> 5 μm) cseppeket állítunk elő. A porlasztógáz legtöbb esetben megegyezik a láng égését tápláló gázzal. Egy pneumatikus porlasztó felépítése látható a 5.2. ábrán. A porlasztó oldalán belépő, nagy sebességű porlasztógáz a porlasztófej végén található keskeny nyíláson kilépve a porlasztó kapillárisában nyomásesést eredményez. Ez egy szívó hatást okozva a mintaoldatot folyamatosan a kapillárisba juttatja. A gázáram nemcsak szívó hatást fejt ki, hanem apró, mikroméretű cseppekre tördeli (diszpergálja) a folyadékot, finom aeroszolt termelve. A ködkamra és a benne elhelyezett terelőlemezek szerepe kiszűrni a nagyobb cseppeket, melyek nagyobb tehetetlenségük miatt nekicsapódva a lemezeknek a lefolyó csövén keresztül távoznak. Ezen a csövön egy vízzárt is kialakítanak.
A pneumatikus porlasztásnál, melynek hatásfoka kb. 10 %, hatékonyabb az ultrahangos vagy a nagynyomású folyadékporlasztás. Az utóbbi hatásfoka vizes oldatoknál 35-50 %, szerves oldószereknél pedig a 90 %-ot is elérheti. A módszer azon alapszik, hogy a folyadékot nagy nyomással (200-300 bar) egy 10-20 µm belső átmérőjű, kör keresztmetszetű furaton átpréselik, ekkor egy vékony folyadékszál keletkezik, amit egy 6-8 mm átmérőjű üveggömbnek ütköztetnek. Az ütközés hatására keletkező bőséges, finom aeroszol jóval homogénebb, mint a pneumatikus vagy az ultrahangos porlasztással kapott aeroszol.
A kellően kicsi, és lehetőleg homogén méretelosztású cseppek a lángba kerülve fokozatosan átalakulnak. Első lépésként a nedves aeroszol szilárd aeroszollá alakul; vagyis a cseppből elpárolog az oldószer, s egy szilárd aeroszol részecske (mikroméretű sókristály) marad vissza. Ez a sókristály aztán megkezdi termikus átalakulását. Először elveszti királyvizét (ha azzal rendelkezett), később megolvad (olvadék aeroszol képződik), majd elpárolog, létrehozva egy molekulagőzt. Az így keletkezett molekulák (melyek lehetnek alap vagy gerjesztett állapotban) a láng megfelelő hőmérsékletű zónáiban alapállapotú atomokká disszociálnak. Ezek a szabad atomok, ha a lánghőmérséklet lehetővé teszi, termikusan gerjesztődhetnek (gerjesztett állapotú atomokká), vagy ionizálódhatnak (alap- és gerjesztett állapotú ionokká). Az ionizáció csökkenti a vizsgálni kívánt komponensek koncentrációját.
Az atomabszorpciós elemzésekhez (FAAS, GFAAS) csak az alapállapotú atomok, míg az atomemissziós elemzésekhez (FES) csak a gerjesztett állapotú atomok hasznosak.
A lángban az eddig leírt termikus folyamatokon kívül egyéb folyamatok is történhetnek, melyek az ionizáción túl szintén zavarják mind az alapállapotú mind a gerjesztett állapotú atomok képződését. Ilyen hatások a mintakomponenseknek a láng redukáló és oxidáló tulajdonságú gyökeivel, molekuláival (O, H, OH, CH, C2, CO2, CO) lezajló reakciói (pl. stabilis oxidok, karbidok keletkezése). Ezek között azonban vannak hasznos reakciók is, melyek segítik az atomizálást (pl. a H, és a C2 gyökök elősegítik a fémoxidok redukcióját).
Az egyik legelterjedtebb atomizáló közeg a láng. A lánghőmérséklet nagysága és a vizsgálni kívánt elem tulajdonságai (legfőképp gerjesztési energiái) befolyásolják, hogy az elem a lángban milyen állapotba kerül. A lánghőmérsékletet függ a lánggázok minőségétől, és azok egymáshoz viszonyított arányától. Az acetilén-levegő lánggal elérhető maximális hőmérséklet 2300 °C, a hidrogén-oxigén láng esetén ez 2700 °C, a dicián-oxigén lángnál pedig 4500 °C. A 2200-3300 °C hőmérséklettartományban tulajdonképpen csak az E < 4.5 eV gerjesztési energiájú színképvonalak gerjeszthetők. Ezért a lángszínképekben a fémes elemeknek csak a kis gerjesztési energiájú, 275 nm-nél nagyobb hullámhosszúságú atomvonalai fordulnak elő.
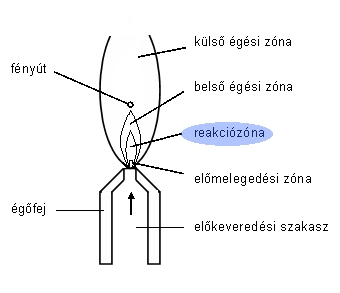
Egy láng szerkezetében (5.3. ábra) kialakuló zónák hőmérséklete eltérő. A legnagyobb hőmérséklete a reakciózónának van. Ez a zóna sok reaktív gyököt tartalmaz, amelyek gerjesztett állapotba kerülve zajforrásként fényt emittálnak, ezért látjuk színét világoskéknek. A reakciózóna fölötti zónák, már kevés reaktív gyököt tartalmaznak és hidegebbek. A fényforrásból származó fény útját (FAAS elemzések esetén!) a külső és belső égési zóna határához irányítjuk, mivel itt keletkezik a legtöbb alapállapotú atom.
A lángok fényemissziója összetett. A legelterjedtebb acetilén-levegő láng emissziós spektruma a következő komponensekből tevődik össze:
A láng alapsugárzásából (a lánggázokból keletkező CH, C2, CN, NH stb. gyökök és az oldószerből, általában vízből, származó OH gyökök sávjaiból),
A lángban gerjesztett atomok és molekulák emissziós spektrumából.
A lángokat sokféle szempont szerint csoportosíthatjuk:
Ha a lánggázokat az égést megelőzően összekeverik, előkevert lángokról beszélünk (ilyen az acetilén-levegő láng; a szénhidrogén-levegő lángok). Ha az égéshez szükséges oxigén a láng környezetében lévő levegőből jut be a lángba, diffúziós lángról beszélünk (ilyen a gyertya lángja).
A gázok áramlásai sebessége szerint megkülönböztetünk lamináris (ahol az áramlást jellemző Reynolds-szám (Re) kisebb, mint 2300) és turbulens lángokat (ahol Re nagyobb, mint 2300).
Az égés sebessége szerint stacionárius, álló láng akkor jön létre, ha az égőn kiáramló gázok áramlási sebessége azonos az égés ellentétes irányú sebességével. Ha az égési sebesség nagyobb, a láng „visszaég”, ha kisebb, akkor a lángot a kiáramló gázok elfújják.
A vizsgált elemre jellemző emittált fényt el kell különíteni a láng alapsugárzásától, illetve a más elemek/molekulák emissziójából származó sugárzástól. Erre szolgálnak a monokromátorok (pl. prizma, optikai rács), melyek kb. 0.01-1 nm szélességű hullámhossztartományt képesek elkülöníteni.
A monokromátoron átjutott fény erősségét legtöbbször fotoelektron-sokszorozóval (PMT) mérik, mely kis intenzitású fény érzékelését is lehetővé teszi. A detektor (itt a fotoelektron-sokszorozó) feladata a fényenergia elektromos energiává alakítása. Régen az emissziós színképet lefényképezték (spektrográfos módszer), de a mérés kis fényintenzitásnál sok időt vett igénybe.
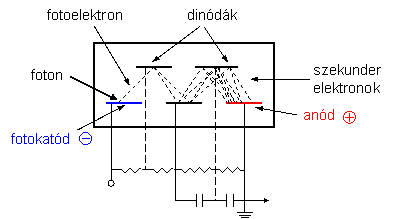
A fotoelektron-sokszorozó (5.4. ábra) tartalmaz egy fotokatódot, több dinódát (8-20) és egy anódot. A fotokatód olyan anyaggal van bevonva, amit ha fény (foton) ér, felületéből elektronok lépnek ki. A katódból fény hatására kilépő úgynevezett fotoelektronok (a katód és az első dinóda közé kapcsolt feszültségesés miatt) az első dinóda felé vándorolnak, és abba becsapódnak. A dinóda felületéből az ütközés hatására szekunder elektronok lépnek ki, melyek száma többszöröse lesz a becsapódó elektronoknak. Az elektronok többszöröződése a következő dinódákon megismétlődik, így egyre több elektron keletkezik, melyek végül az anódba csapódnak. Az elektronok száma exponenciálisan nő a dinódák számával. Ha az anódra érkező elektronok számát elosztjuk a katódot elhagyó elektronok számával, megkapjuk a fotoelektron-sokszorozó erősítési faktorát, mely a 1010 értéket is elérheti.
A gyakorlat menete: Az 50 ppm (1 ppm = 10-6 g/cm3) koncentrációjú K+-törzsoldatból megfelelő hígítással 1, 2, 3, 4 és 5 ppm-es oldatokat készítünk (50,00 cm3-es mérőlombikokban). Ez lesz a kalibráló oldatsorunk.
Beadandó: A jegyzőkönyvben jegyezze fel a kálium-ion mérésénél használt hullámhosszt! Töltse ki a táblázatot! (Ne feledkezzen meg egyes koncentrációkhoz tartozó átlag és szórás értékekről.) Ábrázolja milliméterpapíron a koncentráció (a kalibráló oldatsor koncentrációi) függvényében az abszorbanciák átlagértékeit! Az így kapott pontokra illesszen egyenest manuálisan, illetve számolja ki a pontokra a legkisebb négyzetek módszerével illeszthető egyenes egyenletét! Határozza meg az ismeretlen K+-oldat koncentrációját ppm-ben a manuálisan illesztett egyenes és a kiszámolt egyenes egyenlete segítségével is!
| A1 | A2 | A3 | A4 | A5 | Aátlag | Aszórás | |
|---|---|---|---|---|---|---|---|
| 1 ppm | |||||||
| 2 ppm | |||||||
| 3 ppm | |||||||
| 4 ppm | |||||||
| 5 ppm | |||||||
| ismeretlen |
FES: lángemissziós spektrometria (flame emission
spectrometry) FAAS: lángatomabszorpciós spektrometria (flame atomic
absorption spectrometry) GFAAS: grafitkemencés atomabszorpciós
spektrometria (graphite furnace atomic absorption spectrometry) PMT:
fotoelektron-sokszorozó (photomultiplier tube)
Milyen összefüggés írható fel a fény energiája és hullámhossza között?
Milyen folyamatok játszódnak le a porlasztás során keletkező cseppekkel a lángban?
Milyen fő részekből áll az atomabszorpciós spektrométer és mi az egyes részek funkciója?
Hogyan történik a mintabevitel a lángemissziós technikában?
Milyen típusú részecskéket használhatunk fel az atomabszorpciós és az atomemissziós elemzésekhez; és miért?
Mi a fotoelektron-sokszorozó működési elve?
Rajzolja le a láng szerkezetét!
Mi a lényege és mekkora a hatásfoka a nagynyomású folyadékporlasztásnak?
Milyen területeken használható a lángemissziós spektrometria?